Menurut susunan partikelnya zat dapat dibedakan – Menurut susunan partikelnya, zat dapat dibedakan menjadi padat, cair, dan gas. Perbedaan susunan ini menentukan sifat khas masing-masing zat yang kita jumpai dalam kehidupan sehari-hari.
Mari kita telusuri lebih dalam tentang klasifikasi zat berdasarkan susunan partikelnya, serta sifat-sifat unik yang dimilikinya.
Jenis-Jenis Zat Berdasarkan Susunan Partikel: Menurut Susunan Partikelnya Zat Dapat Dibedakan
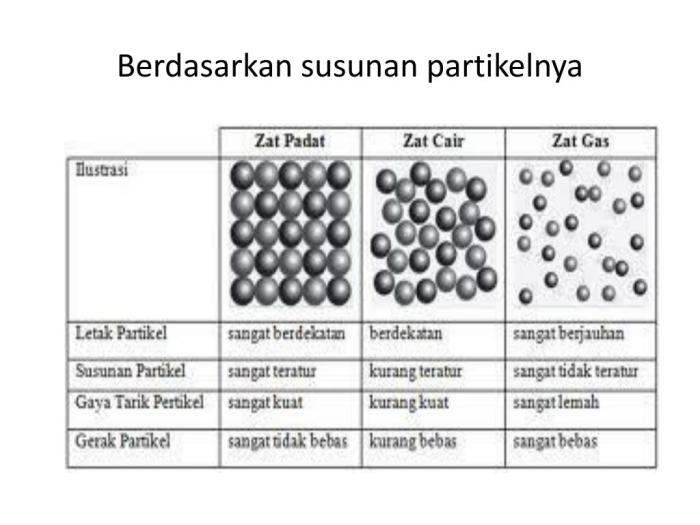
Susunan partikel zat menentukan sifat-sifatnya. Berdasarkan susunan partikelnya, zat dapat diklasifikasikan menjadi tiga jenis utama: padat, cair, dan gas.
Zat Padat
Zat padat memiliki susunan partikel yang rapat dan tersusun teratur. Partikel-partikel zat padat bergetar pada posisi tetapnya, sehingga zat padat memiliki bentuk dan volume yang pasti.
Contoh zat padat antara lain batu, logam, dan kayu.
Zat Cair
Zat cair memiliki susunan partikel yang lebih longgar dibandingkan zat padat. Partikel-partikel zat cair dapat bergerak dan bertukar posisi, sehingga zat cair tidak memiliki bentuk yang pasti tetapi memiliki volume yang pasti.
Contoh zat cair antara lain air, minyak, dan susu.
Zat Gas
Zat gas memiliki susunan partikel yang sangat longgar. Partikel-partikel zat gas dapat bergerak bebas dan tidak memiliki bentuk maupun volume yang pasti.
Contoh zat gas antara lain udara, oksigen, dan hidrogen.
Struktur Zat Padat
Zat padat dicirikan oleh susunan partikel yang rapat dan teratur, yang disebut kisi kristal. Partikel-partikel ini, biasanya berupa atom, ion, atau molekul, tersusun dalam pola berulang tiga dimensi yang stabil. Ikatan yang kuat, seperti ikatan ionik, kovalen, atau logam, menahan partikel-partikel pada posisi tetapnya, memberikan struktur yang kaku dan volume yang pasti.
Ikatan dalam Zat Padat
*
-*Ikatan Ionik
Terjadi antara atom logam dan nonlogam, menghasilkan ion bermuatan berlawanan yang berikatan karena gaya elektrostatik. Contoh: NaCl (garam dapur).
-*Ikatan Kovalen
Terjadi antara atom nonlogam, di mana elektron dibagi untuk membentuk pasangan elektron bersama. Contoh: H2O (air).
-*Ikatan Logam
Terjadi antara atom logam, di mana elektron valensi terdelokalisasi dalam “lautan elektron” di sekitar kation logam. Contoh: Cu (tembaga).
Struktur Kristal
Zat padat memiliki berbagai jenis struktur kristal, antara lain:*
-*Kubus Sederhana
Partikel tersusun pada titik sudut kubus.
-*Kubus Berpusat Badan
Partikel tersusun pada titik sudut dan di pusat kubus.
-*Kubus Berpusat Muka
Partikel tersusun pada titik sudut dan di tengah setiap sisi kubus.
-*Heksagonal Padat
Partikel tersusun dalam lapisan heksagonal berulang, dengan setiap lapisan bergeser seperti sarang lebah.
Sifat Zat Cair
Zat cair merupakan salah satu wujud materi yang memiliki karakteristik unik. Susunan partikel dalam zat cair berbeda dari zat padat dan gas, sehingga memberikan sifat-sifat khas yang membedakannya dari wujud materi lainnya.
Susunan Partikel dalam Zat Cair
Partikel-partikel dalam zat cair tersusun secara acak dan longgar, tidak seperti zat padat yang memiliki susunan partikel yang teratur dan kaku. Partikel-partikel ini memiliki jarak yang lebih besar dibandingkan dengan zat padat, tetapi lebih kecil dibandingkan dengan zat gas.
Sifat-Sifat Zat Cair
- Fluiditas:Zat cair dapat mengalir dengan mudah, menyesuaikan bentuknya sesuai dengan wadah yang menampungnya.
- Kemampuan Mengisi Ruang:Zat cair mengisi seluruh ruang yang tersedia, tidak seperti gas yang hanya mengisi sebagian ruang.
- Tegangan Permukaan:Zat cair memiliki tegangan permukaan, yang menyebabkan terbentuknya permukaan yang cenderung membulat dan meminimalkan luas permukaan.
- Kapilaritas:Zat cair dapat naik atau turun melalui pipa kapiler, melawan gaya gravitasi, karena adanya tegangan permukaan dan adhesi.
- Vektor Transport:Zat cair dapat mengangkut zat lain yang terlarut atau tersuspensi, seperti nutrisi dalam darah atau limbah dalam air limbah.
Aplikasi Praktis Sifat Zat Cair, Menurut susunan partikelnya zat dapat dibedakan
Sifat-sifat zat cair memiliki berbagai aplikasi praktis dalam kehidupan sehari-hari, seperti:
- Pembuatan minuman dan makanan
- Transportasi bahan bakar dan cairan lainnya
- Pelumas dalam mesin
- Penyerap goncangan dalam suspensi kendaraan
- Penggunaan dalam sistem pendingin dan pemanas
Sifat Zat Gas

Zat gas memiliki susunan partikel yang unik yang membedakannya dari zat padat dan cair. Partikel-partikel gas berjarak sangat jauh satu sama lain dan bergerak dengan kecepatan tinggi secara acak.
Ekspansi dan Kompresibilitas
Sifat khas gas adalah kemampuannya untuk mengembang dan dikompresi. Ketika gas dipanaskan, partikel-partikelnya bergerak lebih cepat dan membutuhkan lebih banyak ruang, sehingga gas mengembang. Sebaliknya, ketika gas didinginkan, partikel-partikelnya melambat dan gas dikompresi.
Peran Zat Gas
Zat gas memainkan peran penting dalam berbagai proses:
- Pernapasan:Oksigen, gas yang kita hirup, sangat penting untuk kehidupan.
- Pembakaran:Gas alam, propana, dan gas lainnya digunakan sebagai bahan bakar karena mudah terbakar.
- Industri:Gas seperti nitrogen dan helium digunakan dalam berbagai proses industri, seperti pembuatan baja dan semikonduktor.
Transisi Fasa
Transisi fasa adalah perubahan sifat fisik suatu zat dari satu bentuk ke bentuk lainnya, seperti dari padat ke cair atau dari cair ke gas. Perubahan ini terjadi ketika zat mencapai titik tertentu, di mana energi dan susunan molekulnya berubah.
Faktor-faktor yang Mempengaruhi Transisi Fasa
Beberapa faktor yang mempengaruhi transisi fasa meliputi:
- Suhu:Suhu menentukan jumlah energi kinetik dalam suatu zat. Ketika suhu dinaikkan, energi kinetik meningkat dan molekul bergerak lebih cepat, yang dapat menyebabkan transisi fasa.
- Tekanan:Tekanan dapat mengubah jarak antar molekul, yang dapat mempengaruhi gaya tarik menarik antar molekul dan menyebabkan transisi fasa.
- Komposisi:Penambahan zat lain ke suatu zat dapat mengubah titik leleh atau titik didihnya, sehingga mempengaruhi transisi fasa.
Contoh Transisi Fasa
Beberapa contoh umum transisi fasa meliputi:
- Pembekuan air:Ketika air didinginkan, molekul-molekulnya bergerak lebih lambat dan membentuk ikatan yang lebih kuat, menyebabkan air berubah dari cairan menjadi padat (es).
- Penguapan air:Ketika air dipanaskan, molekul-molekulnya bergerak lebih cepat dan melepaskan diri dari cairan, menyebabkan air berubah dari cair menjadi gas (uap air).
- Kondensasi:Ketika uap air didinginkan, molekul-molekulnya bergerak lebih lambat dan berkumpul bersama, menyebabkan uap air berubah dari gas menjadi cair (embun).